
载脂蛋白E(apo1ipoprotein E,apo E)是乳糜微粒(CM)、极低密度脂蛋白(VLDL)、高密度脂蛋白(HDL)的重要组分。
继人类apoE基因于1973年首次发现后,陆续在小鼠、大鼠、猪、狗、牛、猴子等动物体内也发现了它的踪影。而且在一些动物中,apoE基因的结构有较高的相似性,如人、猪和小鼠的apoE基因均由4个外显子和3个内含子组成。
apoE基因编码的apoE蛋白在稳定微管蛋白结构、细胞内信号传导、免疫调节、糖代谢、氧化应激、脂质代谢及其他细胞过程中发挥重要作用,与人类的衰老,心血管疾病密切相关,apoE基因的多态性及其表达越来越受到研究者的关注,其中小鼠被广泛用作该基因作用机制研究的动物模型。如apoE基因敲除小鼠的出现,增加了一个可用于评估研究人类衰老性疾病的动物模型,它有助于深化研究apoE基因的功能,为多种疾病的治疗提供了药物筛选的平台。尽管小鼠被广泛用作该基因作用机制研究的动物模型,但未见该基因在小鼠各种组织表达的研究报道。本研究通过对小鼠apoE基因表达谱的分析,为小鼠的apoE基因的研究及其动物模型的利用积累基础性的资料。
1、材料与方法
1.1试验动物:健康清洁级昆明种小鼠3只,雌性,40d龄,平均每只体重(28±3)g(广西医科大学实验动物中心提供,批号:06002002001)。处死动物前禁食12h,仅供饮水。颈椎脱臼处死动物,取心、肝、脾、肺、肾、脑、脊髓、胃、小肠、胸腺、肾上腺、胰腺、膀胱、子宫、主动脉、血液、腹肌等17种组织,每样组织标本约100mg,分别放入含有500μLRNA保存液(北京康为世纪生物科技公司)的1.5mLEP管中备用。
组织样本采集均于处死动物后30min之内完成,所用解剖工具和EP管均用0.1%DEPC(北京天根生化科技公司)水浸泡过夜后高温高压消毒。
1.2方法
1.2.1总RNA抽提:总RNA提取选用上述小鼠的心、肝等17种不同组织,取80~100mg组织样在无RNA酶的研磨器中匀浆后采用Trizol-异丙醇(美国Invitrogen公司)沉淀法提取总RNA,1%的琼脂糖凝胶电泳验证RNA的完整性,并于-70℃保存备用,具体操作按照Invitrogen公司提供的RNA提取试剂盒说明书进行。
1.2.2总RNA检测及浓度测定:总RNA的完整性可通过普通琼脂糖凝胶电泳检测。微量核酸蛋白分析仪(美国Quawell Technology.Inc)测量总RNA样品浓度,每个样本重复测量3次,取平均值。
1.2.3总RNA反转录:在经DEPC处理过的0.2mL离心管中加入总RNA,其中:肝RNA取3μL,脊髓、胰腺、心、肺、脾、肾、脑、胃、小肠、胸腺、肾上腺、膀胱、子宫、主动脉、血液和腹肌RNA各取5μL,分别加入1μLOligo(dT)18(100μmol/L)和1μLRandom Primer(100μmol/L)(加拿大MBIFermentas公司),用RNase-freeddH2O将体系补足至12μL。弹指混匀后短暂离心,65℃孵育5min,迅速置于冰上。
向反应体系加入5×MuLVBuffer4μL,d NTPs(10mmol/μL)2μL,Ribolock Inhibitor(5U/μL)1μL,M-MuLV反转录酶(5U/μL)1μL,使反应终体积为20μL,混合均匀并短暂离心,于45℃温育60min,70℃5min以灭活反转录酶,然后放置于冰上冷却。
1.2.4引物设计与PCR扩增:PCR扩增的引物设计参照GenBank中公布的Mus musculus apolipoprotein E的mRNA核酸序列(NM_009696.3),PCR引物由Oligo6.0软件设计,由上海生物工程公司合成。上游引物apoE-F:5’
-gaacaac-ccgcctcgtgacag-3’;下游引物apoE-R:5’
-tggcagtgcgctggcgac-ctt-3’,目的片段的长度为781bp。使用β-actin作为内参,上游引物β-actinF5’
-tgaccggcctgtatgctatc-3’,下游引物β-actinR5’
-tcacatgtctcgatcccagtag-3’,片段长度310bp。PCR反应条件:94℃预变性5min;94℃变性1min,61.5℃退火45s,72℃延伸1min,共35个循环,72℃延伸10min。取PCR产物5μL进行1.5%琼脂糖凝胶电泳,并在凝胶成像系统(美国Bio-Rad公司)上观察扩增效果并照相。
2、结果
2.1 17种组织总RNA的检测:小鼠17种组织总RNA1%琼脂糖凝胶电泳显示出2条清晰的条带,分别为28S和18S,表明总RNA较完好。经微量核酸蛋白分析仪测定,所提取的总RNA在260nm的吸收值与280nm的吸收值比值均在1.8~2.0之间,提示无蛋白质和其他杂质污染,提取的总RNA质量符合实验要求,可用于后续组织表达谱分析。
2.2 小鼠apoE基因组织表达谱分析:将小鼠各个组织反转录获得的cDNA作为模板用于组织表达谱分析。经PCR扩增后,取5μL产物在1.5%的琼脂糖凝胶中电泳。用Im-ageJ2X图像分析软件对3次电泳的图像进行处理和分析,并计算各组织的apoE基因相对表达量。结果显示:在40d龄小鼠的17种组织中,apoE都有不同程度的表达,各组织按相对表达量的大小依次为肝(62.2%)、脊髓(61.8%)、脑(58.0%)、肺(57.1%)、肾(55.4%)、心(55.3%)、脾(48.5%)、胸腺(35.8%)、小肠(29.6%)、胃(22.7%)、膀胱(18.5%)、血液(15.1%)、肾上腺(13.3%)、子宫(10.0%)、胰腺(8.7%)和主动脉(6.0%),但在腹肌(0.0%)无表达(图1)。
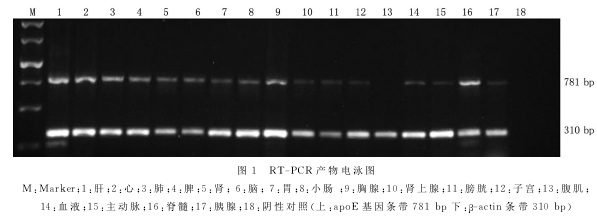
3、讨论
根据GenBank公布的资料,人(GeneID:348)、猪(GeneID:397576)和小鼠(GeneID:11816)3个物种的apoE基因结构都比较相似,均由4个外显子和3个内含子组成,第1,2号外显子都很短且对应的外显子长度都接近,约70bp。尽管这些物种的apoE基因的细微结构存在差异,但毫无疑问它们的功能是一样的,是参与胆固醇和脂类代谢的重要基因。小鼠的apoE基因位于7号染色体,其编码的apoE的氨基酸序列与人的有30%的差异,这些差异多存在于N端和C端,2个物种的apoE受体结合域(136~160bp)高度保守,25个残基中有21个是相同的,但从功能上看,这二者功能的相似度有多大还不清楚。国内外的许多研究都借助apoE基因敲除小鼠作为疾病模型,模拟糖尿病人由于血脂异常导致的神经性病变。用高脂饲料喂养apoE基因敲除小鼠时,小鼠血中胆固醇含量增高而且动脉出现粥样硬化等症状。另外,其巨噬细胞、T细胞和平滑肌细胞的生理反应和人类心血管疾病中的反应极为相似。可见,研究小鼠的apoE基因表达谱可以与人或其他物种的互相比较,从而为apoE基因作用机制积累基础性的资料。
为准确检测apoE基因表达,本研究在小鼠apoE基因的中段设计引物,目的片段长度为781bp,涵盖了apoE基因第1,2,3号外显子的全部和第4号外显子的一部分。结果显示apoE在肝表达量最高,脊髓和脑亦是高表达的组织。小鼠apoE基因在肝和中枢神经组织的高表达,提示这些组织是小鼠apoE的主要代谢场所,该基因在维护中枢神经系统的功能方面起着重要的作用,这与人和猪的apoE基因表达基本相同。
人体很多组织均有apoE合成,除了肝和脑外,肾也是apoE基因高表达区,猪的肾表达显然没有肝和脑的高。而小鼠肾的表达略高于大脑。小鼠和人的心、脾、胃均有表达,但猪的则未见有表达。根据现有的资料来看,小鼠和人的apoE基因表达一致的组织种类多于小鼠和猪。小鼠和人的apoE基因除了4个外显子有很高的同源性外,在基因的5’端约200bp的侧翼序列同样有较高的同源性。造成人、猪和小鼠的apoE表达方面的差异的原因除了遗传构成的原因外,可能涉及到其他调控系统。
人的巨噬细胞也是apoE合成的主要细胞之一,它可以通过合成分泌apoE,参与神经的再生与修复。虽然本研究没有专门分离小鼠的巨噬细胞,但小鼠的胸腺、主动脉和血液中存在着巨噬细胞,所以尚不能断定apoE基因的mRNA是由这些组织的实质细胞还是由其中所含的巨噬细胞产生,或者二者皆参与了apoE基因的表达。
薛越强等在构建人apoE基因的转基因小鼠时,发现人apoE基因在Fl代转基因鼠的多种组织中均有表达,其中最强的表达出现在肾,在脑和心中有中等程度的表达,而肝的表达较少,脾中则近乎没有表达。这与人的apoE基因在肝表达最强、脑次之以及小鼠的肝表达最强、脊髓次之明显不同,这些结果表明,apoE基因在转基因小鼠体内的表达有组织特异性,不同的遗传背景会导致apoE基因的表达谱的改变,在利用小鼠作为研究人类疾病模型时,应加以考虑。
参考文献:
[1]Shore VG,Shore B.Heterogeneity of human plasmavery low density lipoproteins.Separation of species dif-fering in protein components[J].Biochemistry,1973,12(3):502-507.
[2]Mahley RW.Apolipoprotein E:cholesterol transportprotein with expanding role in cell biology[J].Science,1988,240(4 852):622-630.
[3]Reardon CA,Getz GS.Mouse models of atherosclerosis[J].Current Opinion in Lipdology,2001,12(2):167-173.
[4]Horiuchi K,Tajima S,Menju M,et al.Structure and ex-pression of mouse apolipoprotein E gene[J].Journal ofBio1ogica1Chemistry,1989,106(1):98-103.
[5]Weisgraber K H.Apolipoprotein E:structure-functionrelationships[J].Ady Protein Chem,1994,45:249-302.
[6]Lucy M,Hinder,Andrea M,et al.Apolipoprotein Eknockout as the basis for mouse models of dyslipi-demia-induced neuropathy[J].Experimental Neurolo-gy,2013,239:102-110.
[7]Kitagawa K,Matsumoto M,Hori M,et al.Neuroprotec-tive effect of apolipoprotein E against ischemia[J].An-nals of the New York Academy of Sciences,2002,977(1):468-475.
[8] 李仕新,高萍,李加琪,等.猪载脂蛋白E基因的组织表达谱分析[J].四川农业大学学报,2011,29(4):540-543.
[9]Boyles JK,Zoellner CD,Anderson LJ,et al.A role forapolipoprotein E,apolipoprotein A-I,and low densitylipoprotein receptors in cholesterol transport during re-generation and remyelination of the rat sciatic nerve[J].Clin Invest,1989,83(3):1 015-1 031.
[10]薛越强,屠亚军,杨鹏,等.apoE4近交系转基因鼠的高脂血症表现和自发变换行为损害[J].中国生物化学与分子生物学报,2002,18(6):772-775.广西医科大学学报2013Dec;30(6)





