
中国大陆HBeAg阳性慢性乙型肝炎患者比例超过50%。一线核苷类药物治疗的病毒学应答率高,但HBeAg血清学转换率有限;HBeAg清除明显滞后于病毒学应答。发生HBeAg血清学转换是核苷类停药的先决条件。很有必要在治疗过程中预测HBeAg应答情况,以改善患者管理。本研究通过分析拉米夫定或恩替卡韦长期治疗获得维持病毒学应答的患者队列,分析和验证HBeAg持续阳性的潜在预测指标。
资料和方法
一、研究对象
学习队列:2002年1至12月在南方医院肝病中心门诊或病房开始接受拉米夫定(100 mg,葛兰素史克)治疗且获得快速、维持病毒学应答的患者。
验证队列:2007年1月至2012年12月南方医院肝病中心门诊或病房接受恩替卡韦(0.5 mg或1 mg,中美施贵宝)治疗的患者。入组标准:①慢性乙型肝炎或代偿期乙肝肝硬化患者;②治疗基线HBeAg阳性;③规律服药并定期随访(间隔3~6个月),随访时间超 过12个月,每次随访检测血清ALT、HBVDNA、HBeAg、抗-HBe;④恩替卡韦治疗后获得维持病毒学应答,且有病毒学应答后6个月内的HBeAg数据。排除合并其他肝炎病毒感染、HIV感染、服用免疫抑制剂者,或治疗过程中出现病毒学反弹者。
二、主要试剂和仪器
HBeAg和抗-HBe采用Architect i2000全自动免疫发光分析仪(雅培,美国)检测,检测截断值均为1.0s/co。血清HBV DNA定量采用罗氏Lightcycler方法(深圳匹基试剂,检测下限为1000拷贝/mL)。直接测序法确定HBV基因型和HBeAg阴性相关突变。血清ALT正常值上限为40 U/L。
三、定义
病毒学应答定义为治疗后HBV DNA载量低于检测 下 限 (1000拷 贝/mL);HBeAg清除定义为HBeAg效价低于1.0s/co。病毒学反弹定义为获得病毒学应答后连续两次随访HBV DNA>1×104拷贝/mL。快速应答定义为治疗6个月内发生病毒学应答。维持 病毒学应答定义为后续抗病毒 治疗期间HBV DNA持续低于1000拷贝/mL。
四、统计学方法用SPSS13.0及GraphPad Prism5.01软件进行数据计算和统计学分析
HBV DNA及HBeAg数据进行对数化处理后进行统计。计量资料采用均数±标准差或者中位数(范围)表示,正态分布采用独立样本t检验、非正态分布采用非参数检验比较组间差异;分类变量用百分比表示,卡方检验比较组间差异。采用受试者工作特征曲线(ROC)、生存分析及Log-rank检验来确定HBeAg持续阳性的预测指标并判断临界值。双侧P<0.05为差异有统计学意义。
结果
一、学习队列
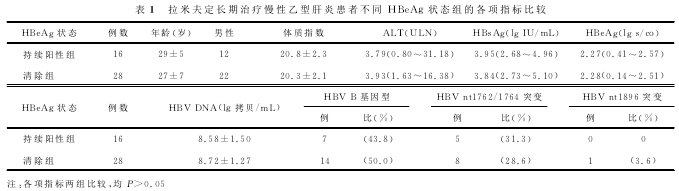
学习队列纳入44例拉米夫定治疗获得快速、维持病毒学应答的患者,观察时间为36个月。期间未能清除HBeAg者16例,占36.4%。性别、年龄、体质指数、基线ALT水平、HBV DNA载量、HBeAg效价、基因型、启动子nt1762/1764和nt1896突变比例等在HBeAg持续阳性和HBeAg清除组间差异无统计学意义,见表1。
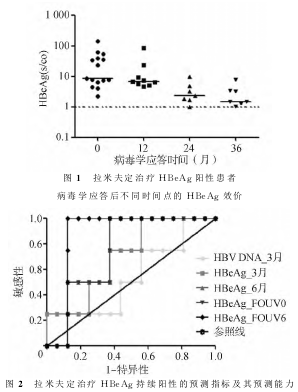
将首次病毒血症不可测 (first onset ofundetectable viremia,FOUV)作为病毒学应答的时间原点。在病毒学应答后0、12、24和36个月时,HBeAg效价的中位数分别为8.5、6.7、2.3和1.5 s/co,同一时间点HBeAg<10.0s/co的 比 例分别为53.3%、77.8%、100%和100%,见图1。说明获得病毒学应答后HBeAg虽未清除,但长期处于较低水平。
ROC曲线提示治疗3个月和6个月的HBVDNA水平及HBeAg效价,包括病毒首次清除(FOUV0)时的HBeAg效价,均不具有预测HBeAg持续阳性的能力。获得病毒学应答后6个 月(FOUV6)的HBeAg效价可作为HBeAg不能清除的预测指标(AUROC=0.875,P=0.023),见图2,表2。根据Youden指数,HBeAg=10.0s/co作为临界值,其敏感性为0.78,特异性为0.71,阳性预测值为0.64,阴性预测值为0.83。以HBeAg效价10.0s/co作为临界值分组行生存分析,HBeAg持续阳性率显著不同(P=0.0093)。见图3。
二、验证队列
长期规律服用恩替卡韦患者171例纳入验证队列,其中慢性乙型肝炎患者153例,代偿期肝硬化患者18例。恩替卡韦初治患者96例,21例曾接受干扰素治疗,40例曾接受其他核苷(酸)类似物(包括拉米夫定、阿德福韦酯、替比夫定)治疗,14例曾先后接受干扰素及其他核苷(酸)类似物治疗。平均年龄33岁,男性148例。获得FOUV的时间为6(3~51)个月,随访时间为21(12~60)个月,其中病毒学应答后的维持治疗时间为15(6~51)个月。
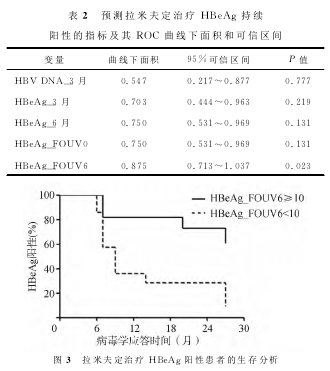
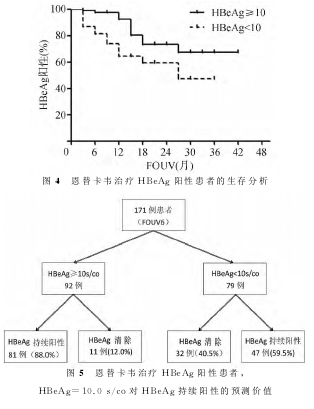
在该验证队列中,病毒学应答后HBeAg持续阳性患者HBeAg长期保持在较低水平,FOUV6和随访期末HBeAg效价中位数分别为18.2和8.5 s/co,(P<0.01);提示虽然HBeAg持续阳性,15(6~51)个月的维持病毒学应答使得HBeAg效价缓慢下降。按FOUV6的HBeAg效价(以10.0s/co为临界点)分组,两组患者HBeAg持续阳性率差异有统计学意义(P=0.005),图4。HBeAg(FOUV6)≥10.0s/co预测HBeAg持续阳性的敏感性为0.63、特异性为0.74、阳性预测值达0.88、阴性预测值为0.40。病毒学应答6个月的HBeAg≥10.0s/co可较准确预测HBeAg持续阳性,图5。
讨论
本研究观察到部分核苷类药物治疗患者很快获得病毒学应答,HBeAg长期维持在较低水平但不能清除。这是核苷类药物长期治疗HBeAg阳性慢性乙型肝炎的一种突出表现,病毒学应答率较高,而HBeAg转换率有限(2年):拉米夫定分别为38.5%、29.2%,恩替卡韦分别为69.8%、38.9%。
即使获得HBeAg血清学应答,2~5年内有66.7%~77.8%的复发率。因此在核苷类药物治疗过程中,对HBeAg持续阳性的预测更有助于临床医生判断患者应答,为长期治疗提供依据。
本研究以拉米夫定治疗获得快速和维持病毒学应答的44例患者作为学习队列,发现在病毒学应答后6个月,HBeAg≥10.0s/co可预测HBeAg不能清除,病毒学应答后24~33个月内64.0%患者无法清除HBeAg。以恩替卡韦治疗队列进行验证:病毒学应答后6个月,HBeAg≥10.0s/co的患者在15(6~51)个月内88.0%不能清除HBeAg。对于病毒学应答患者,无论拉米夫定或恩替卡韦治疗,病毒学应答后6个月HBeAg≥10.0s/co均可有效预测HBeAg不能清除。验证队列与学习队列得出的敏感性、特异性等方面的差异,可能受病毒学应答后随访时间不同影响。两个队列均得出理想的阳性预测值(0.64和0.88)。
维持病毒学应答期间,HBeAg效价缓慢下降,更长期的维持病毒学应答或许会增加HBeAg清除的概率。验证队列病毒学应答后随访时间为15(6~51)个月,提示恩替卡韦治疗获得病毒学应答后6个月的HBeAg≥10.0s/co预测一年半内HBeAg持续阳性可信度较高。我们的预测模型需要更长维持治疗时间及更大样本量的队列进行检验或修订。
在本研究中,用基线及随访资料齐全的拉米夫定治疗队列作为学习队列,全面对比分析了包括年龄、治疗前ALT、HBV DNA、HBeAg、病毒基因型、HBeAg阴性相关突变以及治疗过程中HBV DNA、HBeAg的变化对HBeAg应答的影响,未得出阳性结论,可能与病例的选择(仅仅包括了快速及维持病毒学应答患者)有关。研究中HBeAg持续阳性患者病毒学应答后6个月的HBeAg已处于较低水平,学习队列和验证队列中<100.0s/co的比例分别为100%,75.8%。学习队列中位数为8.37,验证队列中位数为18.25,其中95%患者低于361.4 s/co,可基本排除HBeAg浓度过高致钩状(hook)效应,出现HBeAg假阴性结果可能。
总之,对于核苷类药物(拉米夫定或恩替卡韦)治疗并获得维持病毒学应答的HBeAg阳性慢性乙型肝炎患者,病毒学应答后6个月HBeAg≥10.0s/co可以预测HBeAg持续阳性,为临床医生指导患者长期治疗提供依据。





