�����ؼ��ʣ������ײ�Τ; ������Τ; ֱ�ӿ�����ҩ��; ���Ա��Ͳ����Ը���;
����2006��ȫ��Ѫ�����в�ѧ������ʾ, �ҹ�HCV��Ⱦ��Լ��1000��;����ҽ���������ڶԱ��ε���֪�����, ���������μ���ʵIJ������[1]����ֱ�ӿ�����ҩ�� (direct-acting antivira agents, DAAs) ����ǰ, ���Ҷ���������+����Τ�� (PR) ����һֱΪ�����ı����Ʒ���;����PR�����Ƴ̳�, ���ڷ������������ơ�������ʧ�ߡ���Ѫ��������Ӧ, ��Щ���±��λ��߿��������Ƶ������Բ�, �ʽ��в��ֻ��߽��ܿ���������[2]������DAAs��ҩ����з��ɹ�������, �������ƿ����������ص���ʱ��[3]�����ڹ���ԭ�����Ƶ�DAAs��ҩ��۸���δ�ڹ������е����ԭ��, ����ʵ����, �ҹ��ܶ��ͨ������;����ȡ�������ҩ����ڶԸ���ҩ���ʹ��ȱ������, ��ȫ��ҩ��Ϊһ����ʵ�����е�����;��˱������ڿ�������Է���ҩ����Ч����ȫ������չ���о�, ����Ϊ������ҩ��ȫ���ṩָ����
����1�������뷽��
����1.1 �������
�����ռ�2016��1��—2017��1��������ҽרһ��ԺסԺ����ʹ��DAAs���Ƶ�68�����Ա������ߵ��ٴ�����, ���лع��Է�����������30��, Ů38��;����30��70��, ƽ�� (54±9.14) �ꡣ�ι���������11��, ���Ը���43��, ��Ӳ��������8��, ��Ӳ��ʧ������6��;��ϱ����ձ�������ָ�� (2015���°�) [4]�����г��λ���63��, �����ؾ��� (ͣҩ����/�����ز�����) ����5�������β����������:1b��41�� (60.29%) , 2a��27�� (39.71%) ;HCVRNA����Ϊ5.60E+03��5.90E+07 IU/ml��
����1.2 �����Ʒ���
�������л��߾��ڷ����ײ�ΤƬ (Sofosbuvir SOF) ���ϴ�����ΤƬ (Daclatasvir DCV) ���������ơ�ҩƷ����ӡ��NATCO��˾, �ɻ������д�����ʽ��ȡ���Ǹ�Ӳ�����߲���12 W����, �ڷ�SOF 400 mg/d+DCV 60 mg/d, �Ƴ�12 W;��Ӳ�����߲���24 W����, �ڷ�SOF 400 mg/d+DCV 60 mg/d, �Ƴ�24 W�����ƽ��������12 W��
����1.3�� �۲�ָ��
����(1) ��Ч�۲�ָ��:���ƹ����м��Ѫ��HCVRNA���ι���, HCVRNA��������RT-PCR��, ��ͼ������Ϊ15 U/ml���۲���ٲ���ѧӦ�� (rapid virological response, RVR) :���������ƺ�4 WʱѪ��HCVRNA���ڼ������;���ƽ���ʱ����ѧӦ�� (end treatment virologica response, ETVR) :���������ƽ���ʱHCV RNA���ڼ������;��������ѧӦ�� (sustained virologic response, SVR) �������Ƴ̽�����12 WʱѪ��HCV RNA���ڼ�����ޡ� (2) ��ȫ��ָ��:�Ƚ�����ǰ���Ѫ���桢�����ܡ��ļ�ø�仯, ��ͷʹ����������к�Ȳ�����Ӧ�����ʡ�
����1.4�� ͳ��ѧ����
��������Excel 2003��SPSS 16.0��������ͳ�Ʒ������������ϲ��� (±s) ��ʾ, ����ǰ������ԱȽϲ����������t����;������������ (%) ��ʾ, �����ʵıȽϲ���χ2���顣P<0.05Ϊ�������ͳ��ѧ���塣
����2�� ���
����2.1 ����ѧӦ��
��������������1 W, 19�� (27.94%) ����HCV RNA���ڼ������;4 Wʱ64�� (94.12%) �����RVR;���������ƽ���ʱ67�� (98.53%) �����ETVR;�������Ƴ̽�����12W, 66�� (97.06%) �����SVR����ͬ������֮�䲡��ѧӦ�������ͳ��ѧ���� (P>0.05) , ����1;��Ӳ����Ǹ�Ӳ����IJ���ѧӦ�������ͳ��ѧ���� (P>0.05) , ����2��
������1 ��ͬ������֮�䲡��ѧӦ��Ƚ�[�� (%) ]
![��1 ��ͬ������֮�䲡��ѧӦ��Ƚ�[�� (%) ]](http://www.xueshut.com/uploads/allimg/190603/36-1Z603095150322.jpg)
������2 ��Ӳ����ͷǸ�Ӳ���鲡��ѧӦ��Ƚ�[�� (%) ]
![��2 ��Ӳ����ͷǸ�Ӳ���鲡��ѧӦ��Ƚ�[�� (%) ]](http://www.xueshut.com/uploads/allimg/190603/36-1Z603095131546.jpg)
����2.2�� ����ѧӦ��
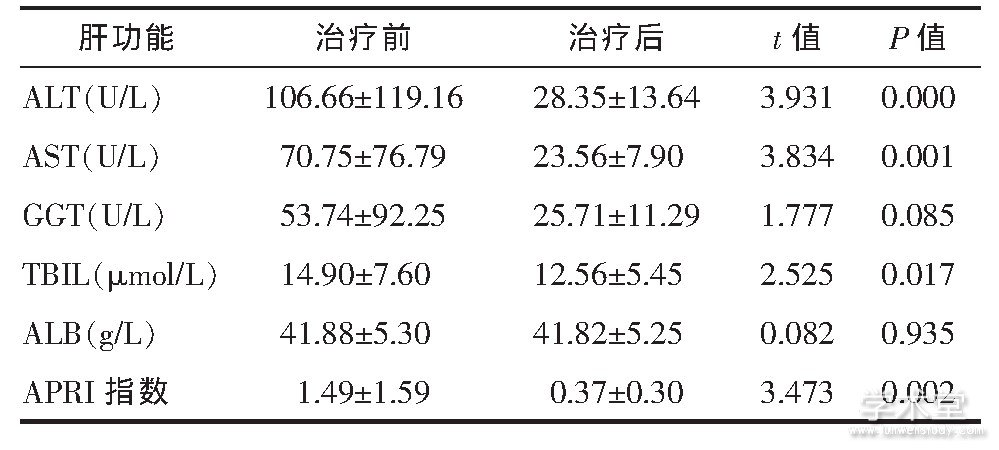
�������ƽ���������ᰱ��ת��ø (ALT) �����Ŷ����ᰱ��ת��ø (AST) �������ؾ�������ǰ�����½�, ������ͳ��ѧ���� (P<0.05) ;���Ը�����Ӳ����, 37�����߸ι��ܸ���, �����ʴ�86.05%��APRIָ��Ҳ�����½�, ������ͳ��ѧ���� (P<0.05) ������3��
������3 ����ǰ��ι��ܼ�APRIָ���ı仯 (±s)
����2.3�� ��ȫ������
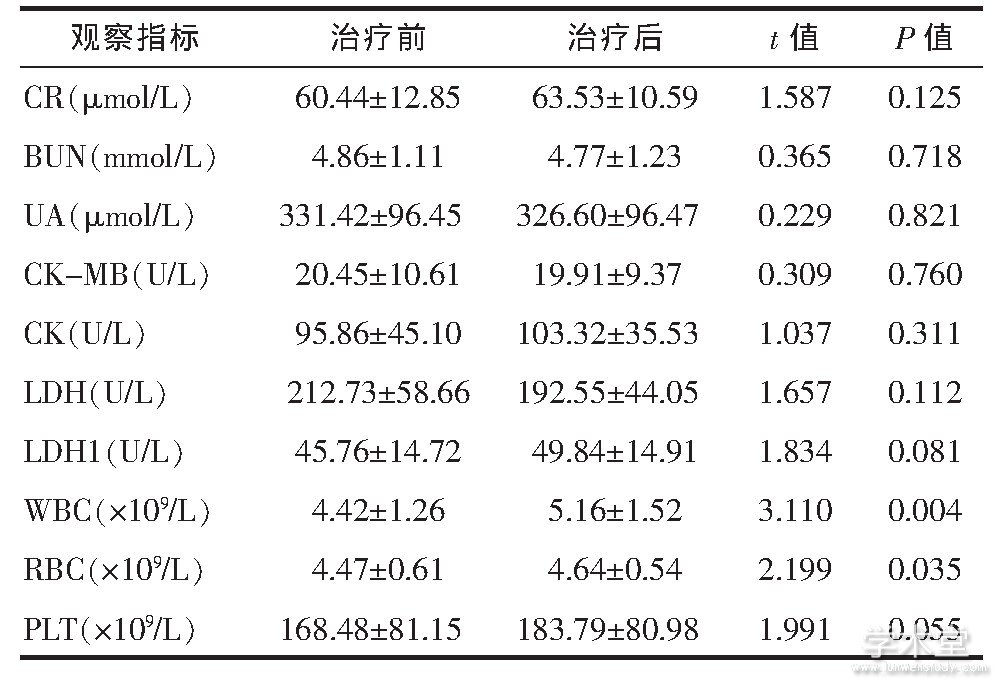
�����������ǰ��Ѫ���桢�����ܡ��ļ�ø�仯�����߲�����Ӧ��1��ʧ�����ڸ�Ӳ�����������ƹ���������������Ѫ��ֹ����, ����߾��������, ��ͣҩ���12 W���ϡ���15������ (22.06%) ������������Ӧ, ����Ϊ����7����ͷ��3����ͷʹ2������к2����Ƥ��1��, ��������, �����л��⡣����ָ�����4��
������4 ����ǰ�������ܡ��ļ�ø��Ѫ����仯 (±s)
����3�� ����
����HCV�����麬��һ�����Ŷ����, ��Ϊ�ṹ�������ͷǽṹ������, �ֱ����ṹ���ͷǽṹ (nonstructure, NS) ���ס��ǽṹ������Ҫ�Dz��벡�����ƵĹ���ø, NS3����Ϊ��������ø��HCVRNA����ø, NS5����ΪHCVRNAָ����RNA���ø, �ڲ����������dz���Ҫ�����á�DAAs��ҩ��ֱ�������ڷǽṹ����, �Ӷ����Ʋ������ơ�������, ��Բ�ͬ�е��DAAs�õ���Ѹ�ٷ�չ, ����NS5A��NS5B����Ҫ���ð�λ����������о�����DAAS��ҩ���������Ա�������Ч�ʸ�, ��ʹ����90%�Ļ���ó�������ѧӦ�� (SVR) [5,6]��
�������ײ�Τ (sofosbuvir, SOF) ��HCVNS5B RNA������RNA�ۺ�ø���Ƽ�, �þۺ�ø�Բ�����������Ҫ���á�SOF��һ�ֺ�����ǰ��ҩ��, ��ϸ���ڴ�лΪ����ҩ�����Ե�������������������, �ɱ�NS5B�ۺ�øǶ��HCVRNA�ж���ֹ�������ơ������ٴ��о�֤ʵ, SOF�������Ա��Ͳ����Ը�����������Ч, ��ȫ������, ��ҩ��ҩ���ϸ�, ����������ȫ��������[7,8]��������Τ (daclatasvir, DCV) ��NS5A����ø���Ƽ�, ͨ����NS5A���ṹ��1��N-�������, ��ʹNS5A���ṹŤ��, �Ӷ�����HCVRNA���ƺ�װ��, ��ǿЧ��HCVҩ��֮һ, ����������ȫ��������[9,10,11]���о��������ײ�Τ�ʹ�����Τ����֮��������ҩ, ����Эͬ����, ������ָ�Ͼ��Ƽ��������������Ա�����[4,12,13]�����о�����, ���ײ�Τ���ϴ�����Τ (SOF+DCV) �������Ա�����, ��Ч����, ����1 Wʱ����27.94%�Ļ���HCV RNA���ڼ������, 94.12%�Ļ����RVR, ���������ƽ���ʱ98.53%�����ETVR, SVR12�ߴ�97.06%, �������о����һ��[14]��1b�ͺ�2a�Ͳ���ѧӦ������;��Ӳ����ͷǸ�Ӳ����IJ���ѧӦ�����졣���ƽ������߸ι������Ը���, ALT��AST�������ؽ�����ǰ�������½�, ALB����;��ʾSOF+DCV���������ƿ��Լ��������֢�����Ƹι��ܡ�
���������о�����, SOF+DCV���Ʊ����ײ�����ӦС, �����Ժ�[14]�����о��۲컼����, ����1��ʧ�����ڸ�Ӳ�����������ƹ���������������Ѫ��ֹ����;����߾�������ơ�22.06%�Ļ��߳���һ���Է�����ͷ�Ρ�ͷʹ����к��Ƥ�����������Ӧ, �����л��⡣���ײ�Τ��Ҫ��������й, �����ж������˻��߲���Ҫ��������[15]�����б���ָ��, ��DAASҩ�����ƹ����пɼ�ALT�����ἤøһ��������[16]�����������ƹ����м�������ܡ��ļ�ø, ��������ǰ�������Ա仯, ����LDH1������ǰ�������, ��������ͳ��ѧ���塣�Ƚ�����ǰ��Ѫ����仯, ���ְ�ϸ������ϸ����ѪС���������ǰ��������, ������ǿ��������ƺ�, �ι��ܸ���, Ƣ���ܿ��������йء�ͬʱ������, ���������ƺ�APRIָ��������ǰ�����½�, ��ʾSOF+DCV���ƿ��Լ������ά���̶ȡ���Ը�Ӳ������, �ڽ��������, �������۲����ά��ָ��ı仯��
���������
����[1]���, �½�, ׯ��.���������в�ѧ[J].ʵ�ø��ಡ��־, 2012, 15 (5) :379-383.
����[2]κ��.�������������Ƶ���ʷ�ͷ�չ[J].�ٴ��ڿ���־, 2013, 30 (11) :727-729.
����[3]ZIMMERMANN HW, TACKE F.The beginning of the end for interferon therapy-novel interferon-free treatment options for hepatitis C.[J].Zeitschrift Für Gastroenterologie, 2014, 52 (5) :450-452.
����[4] κ��, �����.��������ָ�� (2015���°�) [J].����, 2015, 33 (12) :933-949.
����[5] SULKOWSKI M S, GARDINER D F, RODRIGUEZTORRES M, et al.Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection[J].N Engl J Med, 2014, 370 (3) :211-221.
����[6] KEATING GM.Ledipasvir/Sofosbuvir:a review of its use in chronic hepatitis C[J].Drugs, 2015, 75 (6) :675.
����[7] POORDAD F, SCHIFF ER, Vierling JM, et al.Daclatasvir with sofosbuvir and ribavirin for hepatitis C virus infection with advanced cirrhosis or post-liver transplantation recurrence[J].Hepatology, 2016, 63 (5) :1493-1505.
����[8] BECK KR, KIM N, KHALILI M.Sofosbuvir-containing regimens for chronic hepatitis C are successful in the safety-net population:a real-world experience[J].Digestive Diseases&Sciences, 2016, 61 (12) :1-7.
����[9] GAMAL N, GITTO S, Andreone P.Efficacy and safety of daclatasvir in hepatitis C:an overview[J].Journal of Clinical&Translational Hepatology, 2016, 4 (4) :336-344.
����[10] MACDONALD A, HARRIS M.Hepatitis C virus NS5A:tales of a promiscuous protein[J].Journal of General Virology, 2004, 85 (9) :2485-2502.
����[11] BELEMA M, MEANWELL NA.Discovery of daclatasvir, a pangenotypic hepatitis C virus NS5A replication complex inhibitor with potent clinical effect[J].Journal of Medicinal Chemistry, 2014, 57 (12) :5057-5071.
����[12] OMATA M, KANDA T, WEI L, et al.APASL consensus statements and recommendation on treatment of hepatitis C[J].Hepatology International, 2016, 10 (5) :702-726.
����[13]EASL Recommendations on Treatment of Hepatitis C 2016[J].Journal of Hepatology, 2017, 66 (1) :153-194.
����[14] SULKOWSKI MS, GARDINER DF, RODRIGUEZTORRES M, et al.Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection[J].N Engl J Med, 2014, 370 (3) :211-221.
����[15]SAXENA V, KORAISHY FM, SISE ME, et al.Safety and efficacy of sofosbuvir-containing regimens in hepatitis C-infected patients with impaired renal function[J].Liver International Official Journal of the International Association for the Study of the Liver, 2016, 36 (6) :807-816.
����[16]����Ӣ, ʢ���, ����, ��.ֱ�ӿ�����ҩ�����Ʊ�����Ӳ�����ڿ�������Ч����ȫ���ٴ�ʵ���о�[J].��Ⱦ����Ϣ, 2016, 29 (2) :81-84.





