ѪҺ�ڿ����ĵ���ƪ��ѪҺ�������ߵĴ�����װ�����ʹ�����̽��
����ժҪ��Ŀ��:�˽�ij������ҽԺ (���¼��“��Ժ”) ѪҺ�ڿƴ�����װ���������ѪҺ���������������:�ռ�2015��4����2017��4�¸�ԺѪҺ�ڿ�ʹ��ע���ô�����װ����ʻ��ߵĵ��Ӳ���, ����ٴ�����ͳ�ƹ۲�� (ֽ�ʰ�) ��¼�뻼�ߵ��ٴ�����, ����Epidata 3.1���������������ݿⲢ��������ת¼, ���ʹ��Excel����ͳ�����ݡ��Ի����������������Ϣ����ҩǰ������������ˮ���������Ҷ��ƽ�ȼ�����ˮ���ơ�����ҩ�����벻���¼��ȸ��ٴ�ָ�����ͳ�Ʒ��������:������19������ (31����) , ���л��߶������˼����Ҷ��ƽ�ȼ�����ҩ����;�����ڼ�ˮ��������Ϊ87.1% (27����) ;93.5% (29����) �Ļ���ʹ��������ˮ���п�ǻ�Ĥ��Ԥ��������;2�����߷�������������, 1�����߷������ظ�����;���ġ���Ԥ��Ż�¡���ǻ�Ĥ��4���������Ƶķ����ʷֱ�Ϊ22.6% (7����) ��12.9% (4����) ��25.8% (8����) ��48.4% (15����) ������:ѪҺ�ڿƴ�����װ����ʵ�ʹ������Ϲ淶, ������ƻ������һ�����ơ�ҩʦ��ʹ�ö��ַ����Ż�������װ����ʵ�ʹ�á�
�����ؼ��ʣ�������װ�����; Ӧ����״; ����ҩ����; �����¼�;
����Analysis of High-Dose Methotrexate in the Treatment of Hematological Malignancies
����TAN Zhiyuan CHEN Ken LIU Wei WAN Wei HU Kai ZHAO Rongsheng
����Dept.of Pharmacy, Peking University Third Hospital Pharmacy Administration and Clinical Pharmacy, Peking University Pharmaceutical Science Dept.of Hematology, Peking University Third Hospital
����Abstract��OBJECTIVE: To investigate the current status of high-dose methotrexate in the treatment of hematological malignancies in a grade �� level A hospital (hereinafter referred to as “the hospital”) . METHODS: Electronic medical records of patients with high-dose methotrexate for injection in the department of hematology of the hospital from Apr. 2015 to Apr. 2017 were collected. The clinical data observation table (paper version) was designed and the clinical data were recorded. Epidata 3.1 was used to establish the electronic database and transcribe the data. Patients' basic information, treatment information, pre-medication evaluation, alkalization, hydration, calcium folic acid rescue and mouthwash treatment, therapeutic drug monitoring and adverse events were statistically analyzed. RESULTS: A total of 19 patients (31 case-times) were enrolled, and all patients underwent alkalization, calcium folic acid rescue and therapeutic drug monitoring. During chemotherapy, the hydration coverage rate was 87.1% (27 case-times) . And 93.5% (29 case-times) used mouthwash for the prevention and treatment of oral mucositis. There were 2 patients developed severe kidney injury and 1 patient developed severe liver injury. The incidences of nausea, undesired vomiting, oral mucositis, and grade �� myelosuppression were 22.6% (7 case-times) , 12.9% (4 case-times) , 25.8% (8 case-times) , and 48.4% (15 case-times) . CONCLUSIONS: The use of high-dose methotrexate in the department of hematology is generally standardized, and relevant treatment links need to be further improved. Pharmacists can use a variety of methods to optimize the use of high-dose methotrexate.
�����װ����� (methotrexate, MTX) Ϊ�ٴ����õ�Ҷ������, С���� (≤50 mg/m2) ʱӦ����������ؼ��������ʪ�ؽ��ס�����ҩ����>500 mg/m2Ӧ��ʱΪ������װ����� (high-dose methotrexate, HDMTX) , �ɵ���Ӧ�û�����������ҩ����Ӧ��, �����ڼ���Ѫ�����߷����ܰ��� (���ࡢغ���ַ���������) ����������֧���ܷΰ���[1]��Ŀǰ, HDMTX��Ӧ����������������: (1) �����������ԡ�ѪҩŨ�����������Ӱ��, �综�ߵ����䡢�������ܡ�������ȡ��������͡�������ҩ����������������ص�, ����ش�лø�Ļ�����ڻ����̬��, ����������Ҫ��������ҩ���� (therapeutic drug monitoring, TDM) �� (2) ��ҩ���ռ��ߡ�HDMTX����ָ����, ���Խϴ�, �������������ԡ��ζ��ԡ��Ĥ���ԡ�θ�������ˡ��ζ��ԡ�ѪҺ���ԡ����ԡ�Ƥ�����Ժͳ�����Ӧ������ҩƷ�����¼� (adverse drug event, ADE) �� (3) ��ҩ�ϸ��ӡ�HDMTXӦ��ʱ������ҽ���϶�, �漰ˮ���������ҺpH��⡢��עʱ�䡢ѪҩŨ�ȼ�⡢��Ҷ��ƽ�ȼ���������¼�ȡ��ɴ˿ɼ�, HDMTX�ĸ�ҩ��ػ��ڸ���, �ڸ�ҩǰ��������м�⡣�����������ʾ, Ŀǰ���ٴ��о���Ҫ������ѪҩŨ��/����������Ч��������Ӧ��������֮��Ĺ�ϵ[2,3,4,5]�Լ�HDMTX���廯��ҩģ����[6,7,8]��, �������ҩ��ʹ��ȫ���̽�����������������о������о���ij������ҽԺ (���¼��“��Ժ”) ѪҺ�������ߵ�HDMTXʹ��������лع��Է���, ���ڶ�HDMTX��ҩȫ���̽��и���Ч�Ĺ���, �淶HDMTX��ҩǰ������������ҩ�������ҩ������TDM���ȵ�, ���HDMTX���丨��ҩ���ٴ�Ӧ�õ���Ч�Լ���ȫ�ԡ�
����1 �����뷽��
����1.1 ������Դ
�����о�����Ϊ2015��4����2017��4�¸�ԺѪҺ�ڿƵ�סԺ���ߡ������:�������ΪѪҺϵͳ�������� (����ϸ����̬ѧ��������֯��ѧ��ϸ���Ŵ�ѧ���������ѧ���) , �����ܰ���/��Ѫ������������ȷ�����������ַ�֤�� (���Լ�Һ�������ϸ���������ӷ��������ϲ�������ʾ������ڸߴ�л�����) ;����HDMTX��ҩ���ƻ����ϻ��ơ����о����������估���塣
����1.2 ����
����1.2.1 �����IJ�������� (case report form, CRF) :
�������ջ����������������Ϣ����ҩǰ���������ά����B��ˮ������Ҷ��ƽ�ȡ�TDM��ADE��8��ģ�����CRF, ���徭ѪҺ�ڿ��ٴ�ҽʦ���ٴ�ҩʦ����, �����ѡȡ3�����ߵ�������Ϣ����Ԥ��, ȷ��CRF�ո塣
����1.2.2 ��дCRF:
������ѪҺ�ڿ��ٴ�ҩʦ������¼�л�ȡʹ��HDMTX���ƵĻ��߲����ż�����, ��ҽԺ��Ϣϵͳ (hospital information system, HIS) �е�ȡ����סԺ���������õ���¼�� (̸־Զ) ��˫�˺˶� (�¿ҡ�̸־Զ) �ķ�ʽ��дCRF����������, Ѱ������� (��ά) �����
����1.2.3 ��Ʋ�¼��������ݿ�:
��������Epidata 3.1��������HDMTX����ѪҺ�����ع����о��������ݿ�, ��Ϣ��¼������CRFһ��, �������Ͱ�����ֵ�͡��ַ��ͺͲ�����������¼�� (̸־Զ) CRF�е�����, �ڽ���˫����� (�¿ҡ�̸־Զ) У�Ժ�, ����, ������¼����Ϻ�, ���ݵ���ΪExcel����
����1.2.4 ����ͳ�������:
�������ղ���������Ϣ��������Ϣ����ҩǰ�������ˮ������Ҷ��ƽ�ȼ�����ˮ������ά����Bʹ�������TDM����Լ�ADE���, ��ģ��ͳ�Ƹ�ԺѪҺ�ڿ�HDMTXӦ����״��
����2 ���
����2.1 ���ߵĻ�����Ϣ�����Ʒ���
�������о�������19�� (31����) ����, ����12��69��, ��λ����40��;���Ի���14�� (ռ73.7%) ��HDMTX��ʹ��31����, MTX��ע������ΧΪ0.81��3.36 g/m2, 10���� (ռ32.3%) �ﵽ��ԭ���Ʒ���Ҫ���MTX����;18���� (ռ58.1%) ����24 h������ע, ����15����ʹ���˸��ɼ���;����, 10���� (ռ32.3%) ����3 h������ע�����ߵĻ�����Ϣ�����Ʒ�������1��
������1 ���ߵĻ�����Ϣ�����Ʒ���
����2.2 ��ҩǰ����
����19��������, 12�� (ռ63.2%) �����˻����⡣����, �Ǽ�����Ҷ�ỹԭø (5, 10-methylenetetrahydrofolate reductase, MTHFR) 677��1298λ���ΪҰ���͵IJ�����Ϊ0;MTHFR 677Ұ����1��, ռ8.3%;MTHFR 1298Ұ����8��, ռ66.7%;ATP��Ϻ�B�Ǽ����Ա1ת�˵����� (ATP-binding cassette subfamily B member 1, ABCB1) 3435 CC��3��, ռ25.0%�����л������ڵĻ��߾����ظ�ˮ����IJ���;5���� (ռ��������31���ε�16.1%) �ڻ���ǰ�����ڼ�ʹ����ά����C;���л����ڻ���ǰ���������ھ�δʹ�ûǰ���ҩ������忹��ҩ������ɳ�ǡ������������ù�����ҩ�
����2.3 ���ˮ��
����2.3.1 �:
�������л������ڵĻ��߶��ڻ���ǰ�� (��) �����ڼ���˼����;96.8% (30����) �Ļ������ڶ��������MTX������ϡ�31���λ�����, 29���� (ռ93.5%) �ڻ��Ƶ��� (D1) ʹ���˾���̼������;21���� (ռ67.7%) ��MTX��ҩǰ1�� (D0) ��ʼ�����ϸ�ı���D1�������ڼ���ҺpH≥7.0, �ڴ˱���, ��15���λ��� (ռ48.4%) ��D1�ⶨ��pH, ���11����, �����Ϊ73.3%;D1��, ��2���λ��� (ռ6.5%) ������ҺpH�쳣��
����2.3.2 ˮ��:
����31���λ�����, 27���� (ռ87.1%) �ڻ���ǰ�� (��) �����ڼ�ִ����ҽ����¼������, D0��¼������4���� (ռ12.9%) ��ˮ���ϸ�ı���D0��MTX�������ڼ�������Ӧ≥2.5 L/m2������δ��¼�������Ļ���, �����������侲������+��ʳ����Һ����2 L���㡣12���λ��� (ռ38.7%) ��D1��MTX�������ڼ�ˮ�������, 1���λ��� (ռ3.2%) ��D0ˮ������ꡣ
����2.4 ��Ҷ��ƽ�ȼ�����ˮʹ�����
����2.4.1 ��Ҷ��ƽ��:
����31���λ�����HDMTX��ҩ���������Ҷ��ƽ��;����, 21���� (ռ67.7%) �ڸ�ҩ��36 h�ڽ��, 7���� (ռ22.6%) �ڸ�ҩ��24 h�ڽ��, 1���� (ռ3.2%) �ڸ�ҩ��16 h�ڽ��;30���� (ռ96.8%) ��ʼʱ���þ�����Ҷ��ƽ��;20���� (ռ64.5%) ��ȴ��;28���� (ռ90.3%) ������MTX������ϡ�
����2.4.2 ����ˮʹ�����:
����29���λ��� (ռ��������31���ε�93.5%) ʹ��������ˮԤ�������ƿ�ǻ�Ĥ��, ����28���� (ռ96.6%) ������ˮ�䷽�ж�ʹ������Ҷ���, ��1���� (ռ3.4%) ������ˮ�м�������ϸ��-����ϸ������̼����ӡ�
����2.5 TDM���
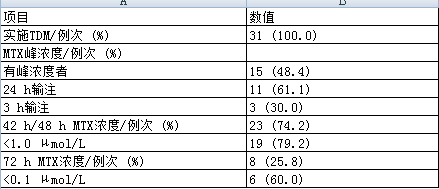
����31����ʹ��HDMTX�Ļ��߶�������TDM, 15���λ��� (ռ48.4%) �����MTX��Ũ��;24 h��ע���߷�Ũ�ȼ�����Ϊ61.1% (11/18) , 3 hΪ30.0% (3/10) ;24 h��ע���MTX��λ��Ũ��Ϊ25.26 μmol/L (9.20��38.72 μmol/L) , 3 h��ע���MTX��λ��Ũ��Ϊ260 μmol/L (260��298 μmol/L) , ����2����Ҫ˵������, 23���λ����ڿ�ʼ��ҩ��42��48 h������ѪҩŨ�ȼ��, ����19����MTXѪҩŨ��≤1 μmol/L, ��������1���λ���δ�ⶨ42��48 hѪҩŨ��, ����60 hʱMTXѪҩŨ��>1 μmol/L, ��48 hʱMTXѪҩŨ�ȴ����Ϊ79.2% (19/24) ;8���λ����ڿ�ʼ��ҩ��72 h������ѪҩŨ�ȼ��, ����4����MTXѪҩŨ��≤0.1 μmol/L, ��������2���λ�����42/48 h��MTXѪҩŨ�Ⱦ���≤0.1 μmol/L, ��δ�ⶨ72 hѪҩŨ��, ��72 hʱMTXѪҩŨ�ȴ����Ϊ60.0% (6/10) ��
������2 TDM���
����
����2.6 ADE�������
����ADE�����������3��
������3 ADE�������
����ע:“—”��ʾ�ζ��Լ���������ָ�겻��һ, ��ָͬ�겻�ܺϲ�ͳ��
����Note:“—”means that indicators of hepatotoxicity and myleosuppression are not single, and different indicators cannot be combined for statistics.
����3 ����
���������о��������, MTHFR 677����ͻ���벻����Ӧ�����������[9]�����о���, ��8.3%�Ļ���MTHFR 677ΪҰ����, ��ʾ�ֻ��ߴ���ͻ��, �ٴ�Ӧ��HDMTXʱ�����м��������ܼ���ǻ�Ĥ�������
��������24 h������ע, �Ƽ���ȡ���ɼ���, ���Ը���شﵽ��̬ѪҩŨ���Է���ЧӦ[9]�����о���, 24 h������ע�Ļ�����, 83.3% (15����/18����) �Ļ���ʹ���˸��ɼ��������ڸ��踺�ɼ������ٴ��Ͻ�����ʵ��, �ʺ���Ӧ��һ�����24 h������עʱ���ɼ�����ʹ���ʡ�
�������о���, ��HDMTX��ҩǰ, 4��Ѫ����ָ��������Ļ���ռ41.9%;5��ι���ָ��������Ļ���ռ51.6%, ָ���쳣�Ļ��߾�Ϊ����쳣��HDMTX����ѪҺ���Ժ����[1], Ӧ��Ѫ���漰�ι���ָ���������ٽ��и�ҩ��
��������ҩ��Ӱ��HDMTX����й[10], ��HDMTXӦ���������ҩ����á����о���, 5���λ�����ʹ��HDMTX����������Ӧ����ע����ά����C��ˮ����ά����, ��δ������Ӧ������Ӱ��HDMTX��й��ҩ�� (�����ӱ����Ƽ�[11]����������̹[12]�������ǰ��ס���[13]��) , ���ܵ�ԭ����ά����C�ڻ��ƻ�����ʹ�ù㷺, �ױ�ҽ����Ա���ӡ����, ��ʹ��HDMTX�����ڼ�Ӧ��ǿ����ά����C��ˮ����ά����ʹ�õĹ�ע��
�������о���, ���еIJ����������˼��96.8%�Ļ��߳�����MTX�������, 93.5%�Ļ�����D1ʹ���˾���̼������, ����67.7%�IJ�����D0ʹ����̼�����ơ���ҺpH���жϼЧ����ָ��, ���ڸ�ҩǰ51.6%�Ļ���δ������ҺpH���, ���м���15���λ�����, �����Ϊ73.3%���ɼ�, ��D0�ļ�Լ���ҩǰ��ҺpH�IJⶨ�ȷ�������Ҫ��ǿ�����о������ʾ, 87.1%�Ļ��߽����˳������ļ��, ����38.7%�Ļ����ڻ����ڼ�ˮ�������, ��1��������D0ˮ������ꡣ���շ������������˵�2��������, 1��������D0δ����ˮ��, ��1��������D2—D3ˮ��������ꡣ����HDMTXʹ�ù�����, Ӧ��D0��ʼ��ǿˮ������¼��������
�������о������ʾ, ��Ҷ��ƽ���ʴ�100%, ����96.7%�Ļ�����ʼ���þ�����Ҷ��ƽ��, 90.3%�Ļ�����24��36 h�ڽ����˽��, ����64.5%�Ļ��߽�ȼ������;����ˮʹ����Ϊ93.5%, ����90.3%�Ļ���ʹ�õ�����ˮ�к���Ҷ���, ����D1����ʼʹ������ˮ�Ļ��߽�ռ12.9%, ��ӦЭ���ٴ�ҽʦ���D1����ˮ��ҽ�������ʡ�
�������42/48 h��72 h MTXѪҩŨ�ȵ�����������ʾMTX�Ƿ�������[1]���ܶ��û��������ʱ�����MTXѪҩŨ��, ��ԭ����������ʱ����ڷǹ�����, ����ʱ���MTXѪҩŨ�ȡ����, �����Ż�MTX��ҩʱ��, ȷ���ܹ���ʱ���MTXѪҩŨ�����ݡ�
����4 ����
�������о������ʾ, ѪҺ�ڿ��ٴ�ҩʦ��HDMTXʹ�ù��̵Ķ�����ھ�Ӧ���и����������Ԥ, ��ά����C������Ӧ�á��ʱ����ˮ��ʱ����ˮ��������ҺpH��⡢��������⡢����ˮʹ��ʱ����ѪҩŨ�ȼ��ȡ�
�������о��ռ���HISϵͳ��HDMTX��ػ�������, ���Դ�����������С������;����ָ���ȡ��������, ���ǻ�Ĥ�ס����ļ�Ż�µij���������Ӧ�¼����۱��ּ�ȱ������֧��;δ��Բ�ͬ��Ԥ��ʩ�Ի��߽��ָ���Ӱ�����ͳ�ƺͷ�����δ��Ӧ������ʵ�����о��ķ���, �ռ�����ߵ�������Ϣ, ����չ�����о��Ͳ��������о�, Ϊ���ڻ��ߺ���Ӧ��HDMTX�ṩ����Ŀ�ѧ���ݡ�
����Ŀǰ, HDMTX�Ĺ淶ʹ���ڹ�����û�ж���, ���ܸ�ҽԺ������Ӧ��Ժ����ҩ�淶, ��������Ƿ�ѡ����, Ϊ��һ���淶HDMTX���ٴ�����Ӧ��, ȷ��HDMTX����Ч�밲ȫ��, ҩʦ����Ӧ��ǿ�ٴ�ʵ������, ��Ӧʹ��������һ���Ż�, ����Ը�����ҩ���ӵ�ҽ���ƶ�ҽ��ģ��, �����е���ҩ������ٴ�ָ���ƶ������� (�籾�����������й�ҩ��ѧ��TDM�о�רҵίԱ��ǣͷ���ƶ�HDMTX�ٴ���ҩָ��) , ��֤�����ٴ�ʵ���л����, ���̶ȸ��ƻ��ߵ��ٴ���֡�
���������
����[1] LaCasce AS.Therapeutic use and toxicity of high-dose methotrexate[DB/OL].Wolters Kluwer.2018.[2018-01-31] (2019-02-14) .https://www.uptodate.com/contents/therapeutic-use-and-toxicity-of-high-dose-methotrexate?search=Therapeutic%20use%20and%20toxicity%20of%20high-dose%20methotrexate&source=Out%20of%20date%20-%20zh-Hans&selectedTitle=1��68.
����[2] κӯӯ, ���՜�, ��˼, ��.������װ��������ƶ�ͯ�����ܰ�ϸ����Ѫ����ѪҩŨ���벻����Ӧ�������[J].�й�ҽԺҩѧ��־, 2014, 34 (22) :1915-1918.
����[3] ����.������װ��������ƶ�ͯ��Ѫ��ѪҩŨ������Ч�Ĺ�ϵ[J].����ҽѧ, 2018, 24 (31) :161-162.
����[4] Hegyi M, Arany A, Semsei AF, et al.Pharmacogenetic analysis of high-dose methotrexate treatment in children with osteosarcoma[J].Oncotarget, 2017, 8 (6) :9388-9398.
����[5] Wang CP.Monitoring and Treatment of Acute Kidney Injury in Chil-dren with Acute Lymphoblastic Leukemia After High Dose Metho-trexate Chemotherapy[J].Iran J Pharm Res, 2016, 15 (4) :957-961.
����[6] �ž�, ����, ��ޱ, ��.������װ������ڼ����ܰ�ϸ����Ѫ�������е�Ⱥ��ҩ��ѧ[J].�й�ҽԺҩѧ��־, 2007, 27 (8) :1061-1065.
����[7] ����, �Ż���, ��˼�, ��.Ӧ���˹�����������������װ����ʻ��ƺ�Ĺ�������[J].�й��ִ�Ӧ��ҩѧ, 2017, 34 (6) :881-887.
����[8] Mei S, Li X, Jiang X, et al.Population Pharmacokinetics of High-Dose Methotrexate in Patients With Primary Central Nervous System Lymphoma[J].J Pharm Sci, 2018, 107 (5) :1454-1460.
����[9] Ettinger LJ, Chervinsky DS, Freeman AI, et al.Pharmacokinetics of methotrexate following intravenous and intraventricular administra-tion in acute lymphocytic leukemia and non-Hodgkin's lymph-oma[J].Cancer, 1982, 50 (9) :1676-1682.
����[10] Hande KR, Balow JE, Drake JC, et al.Methotrexate and hemodialysis[J].Ann Intern Med, 1977, 87 (4) :495-496.
����[11] Suzuki K, Doki K, Homma M, et al.Co-administration of proton pump inhibitors delays elimination of plasma methotrexate in high-dose methotrexate therapy[J].Br J Clin Pharmacol, 2009, 67 (1) :44-49.
����[12] ������, ����, ���, ��.��������ǰ��ա��װ����ʾ�����ע��ҩ��Ũ�ȼ�⼰������о�[J].�л�ѪҺѧ��־, 2012, 33 (12) :1049-1051.
����[13] Thomas MH, Gutterman LA.Methotrexate toxicity in a patient rec-eiving trimethoprim-sulfamethoxazole[J].J Rheumatol, 1986, 13 (2) :440-441.
����鿴>>ѪҺ�ڿ����ģ����㷶��8ƪ����������







