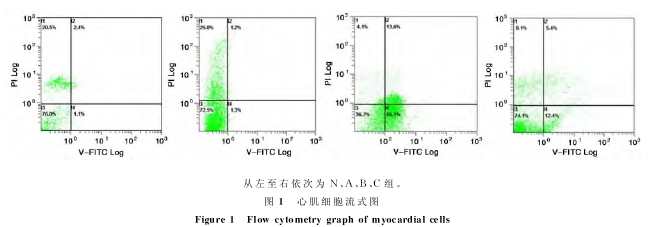
����ȱѪ�ٹ�ע���˵ĸ����ڣ����������ɣʣ����������������ƽ�Ϊ���ӣ����������ɻ����Ƴ��ء�������л�ϰ����й��⣬������Ϊ��ϸ������Ҳ�������й�ϵ��ϸ�������������Ի�ijЩ�����շ��ij���ϸ������������ϸ���źŴ���ͨ·������ȫ���ˡ������о���������ԭ�����ø�� �壨�ͣ��Уˣ���һ����Ҫͨ·�������䳬�����Ա�𣳣��ͣ��У��������������õ��о����١����о�ͨ�� �� �� ȱ Ѫ �� �� ע �� �� ϸ �� ģ �ͣ�̽ �֣𣳣��ͣ��У����ļ�ϸ��ȱѪ�ٹ�ע�����е����á�
�����������뷽��
������������Ҫ�Լ�������
������������������֣��ƣɣԣ�ϸ����������Լ��У��𣳣��ͣ��У����Ƽ������ԣӣ����ṫ˾���ӣ£����������������ȵ��� ø ���ǣ����� ����������ţѪ�� ���ǣ������������ģͣţ������������ǣ����ǣ�������������������������ण��ӣ����ᣬ�����������ͽ�ԭø���ӣ����ᣬ��������α�����Ƽ�����������¡���壨�����������������α���ӣ������ӣ��£�������֯��ѧ�Լ��У��ģ�����ɫ�Լ��У����Ա�������ɭ��˾���ں��ģ���Ⱦɫ�Լ��С����������� ɫ Һ������������ ɫ Һ����ӫ �� �� �� �� �����ã��졡�ڣţɣӣӣ����������ã��졡�ڣţɣӣӣ��������������ϣ̣٣ͣУգӡ��ԣϣˣ٣ϣ�����ʽϸ���ǣ��£ţãˣͣ��Σãϣգ̣ԣţҡ��ţУɣãӡ��������ᣩ��
����������ϸ������������
����ѡȡ����������ӣ��������������¿���ȡ���࣬���ļ���֯���ں��Уģͣţ�Һ�ģ��������������У����ۿƼ��������Ҽ��ɣ�����������֯��飬���룵������ģ����������ȵ���ø��Һ�����Ⱥ��ã�������������������������ú���������Һ���ڣ����������Ĺ����ã����������������ţѪ��ģģͣţ�����Һ��ֹ�������ظ��������̣������Ρ�
�������������������ԣ���������×�����ģ��������������ϸ�������ڣ����� �ǣ����Ѫ������Һ�У������ڣ����������������ڣ�����������������������裬��������ϸ����Һ���ԣ�������������ܶȷֱ�������������������������ã����桢�����ãϣ���������������
�������������Ҹ�������Һ����С�����ļ������ԣͣȣãᣯ�ɣ����ԣ�ɿ��壨�����ã������ͣ��ã����ֱ�ϡ�ͣ��ڣ��������ҹ��Ȼ��ֱ��ãƣɣԣñ�ǵ�ɽ��С��ɣ�Ǽ�������ǵ�ɽ��С��ɣ�ǿ���������衣���ѡȡ��������Ұ��ӫ�������¹۲죬����ӫ��ȾɫΪ��ɫ��ϸ��Ϊ�ļ�ϸ��������������
�������������鼰ģ�ͽ���
����ȡԭ�������ڣ�����ļ�ϸ������×���������ܶ���ֲ�ڣ�����������ƿ�У��������ɹ����ļ�ϸ������ֳ�ȱѪ�飨���飩��ȱѪ�ٹ�ע�飨���飩���У����ͣ��У�������Ԥ�飨���飩�Ϳհ����飨���飩��
�������飺��ģ��ȱѪҺ�ڵ����б��ͣ������������Һ����ģ��ȱѪҺ��ͨ�룱�����������������������Ϸ��ƿ�ڣ���������������������裻���飺��ģ���ٹ�עҺ�������б��ͣ����ȱѪ�������ϸ������ƿ�е�ģ��ȱѪҺ���������뾭������ �ϣ��ͣ��� �ãϣ��Ļ�����履�ͣ����ģ���ٹ�עҺ����ͨ�룹���� �ϣ��ͣ��� �ãϣ��Ļ�����壱��������Ѹ�ٷ��ƿ�ڣ�������������������裻���飺����𣳣��ͣ��У����Ƽ��ӣ£���������������������죯�̣���������Ԥ���������������գ�����������
������������ʽϸ���Ǽ���ļ�ϸ��������
�����������ļ�ϸ���������ãģ��������Һ��ϴ���飬Ȼ����룰�������������ȵ���ø�����ļ�ϸ���������������͵���ʽϸ����������ʽ������ɢ��ͼ����������ʾ����ϸ��������������ʾ��ϸ��������������ʾ����ϸ�������ڵ���ϸ��������������ʾ���ڵ���ϸ����
�������������ף������������������
�����𣳣��ͣ��У˵��ױ����õ����ѽ�Һ��ȡתȾ�������̼���ϸ�����ף��ã������۱�����������Ӿ���������ֵ�Ӿ��������ﵽ�����ĵײ��������ֹ�ҹ��ת����������άĤ�ϣ���������֬�̷۷��Һ��գ��裬���룱�ã�������������¡���壬���������ҹ�����������������ӵĶ������·������裬����£ãɣУ��Σ£���ɫ���ãǣģӣ���������������ϵͳ����ͼ�������
����������ͳ��ѧ����
�������ãӣУӣӣ�������ͳ������ͳ�����ݣ����������ԫ���±���ʾ�������Ƚ�ʹ�ã�����Ƚϡ�����Ƚ�Ӧ�õ����ض��鷽����������Σϣ֣����������ã���顣
���������
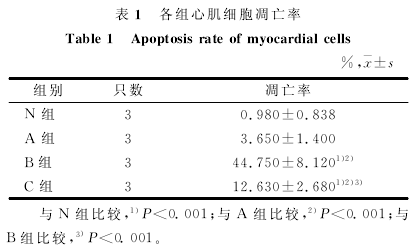
���������������ļ�ϸ�������IJⶨ���
���������ļ�ϸ�������ʼ�������ϸ����ʽͼ��ͼ����
����
�����������ļ�ϸ������
�����𣳣��ͣ��У˵��ױ�������ļ�ϸ���𣳣��ͣ��У˵��ױ����������ͼ����
��

����������ϸ��������𣳣��ͣ��У˵��ױ�������������Է�����ʾ��ϸ��������𣳣��ͣ��У˵��ױ��������أ��������������У�������������
����������
���������о�������������ϸ����ȱѪ�ٹ�ע���˹����е���Ҫ������ʽ��ϸ����ȱѪ�ٹ�עʱ�������ϸ�����ӣ����������ź�ͨ·������ϸ���ĵ���������ϸ���ڵ��ź�ת��;��Ŀǰ�Բ�ʮ��������𣳣��ͣ��У˵ļ������ļ�ȱѪ�ٹ�ע�������ź�ת����һ����Ҫ���ڣ��𣳣��ͣ��У��ź�ͨ·�����������ữ�ȼ����ף������ȣӣУ��������ͣ��У˸��ż� ø�����ͣΣˣ�����ͣΣˣ���ϸ �� �� �� ֬ ø��������У̣������ȵ��ͬʱ��ϸ�����ڴ����źţ����ữ�ͼ�����ֵ���ø��ת¼���ӣ���˿��ԭ��Ӧ������ĵ���ø�����ͣӣˣ�����Ѫ����Ƥϸ���������ӣ��֣ţǣƣ��ȡ����أģΣ���ת¼������������ֳ���ֻ��������ȣ����ձ���Ϊ�������˺��ӻ��������ֲ�ͬ������ѧЧӦ��
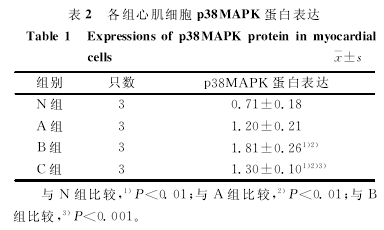
����Ŀǰ���𣳣��ͣ��У��ڵ����е������������ۡ����о��������ļ�ȱѪ�ٹ�ע��𣳣��ͣ��У˿��Դ�������ȣ�𣲣����ٽ�ϸ��Ӧ��ʱ���ҵļ�����������ʹϸ�����ͱ����������Ӷ����ļ�ϸ�������������á���Ҳ���о�֤ʵ���𣳣��ͣ��У���ȱѪ����Ե��ڣͣ��У˼����ø�������������壭��������������������壭�����ļ���ͣԣΣơ��ɣ̣���β���ɣ̣��������ɣ��Ӷ��鵼�����������ļ����ܵļ��ˡ��ˣ�������о����֣��𣳣��ͣ��У˵ļ����𣳣��ͣ��У˻���Ĺ��ȱ����ʹȱѪ�ٹ�ע������ļ�ϸ�������������ӣ��Ĺ��ܽ��͡���ʵ�����֮���Դ��ڲ��죬������𣳣��ͣ��У˼���������ڲ�ͬ�ĵ����Щ�ٵ������P���Ƶ������ﲻƽ���йأ�Ҳ�п���Ϊ���������о�����Ϊ�ó������ӣ𣳣��ͣ��У˻����������о����ڲ����йء�
�������о��������ļ�ϸ����ȱѪ�ٹ�ע�����У��𣳣��ͣ��У˱������Ϊ�𣭣𣳣��ͣ��Уˣ�����ȱѪ��Ͷ���������������ʹ�ã𣳣��ͣ��У����Ƽ���𣳣��ͣ��У˵Ļ���ż��٣��������š���ʾȱѪ�ٹ�ע���̿�ʹ�𣳣��ͣ��У����ữΪ��������ѧ���Եģ𣭣𣳣��ͣ��Уˡ��о���ʾ��ȱѪ��϶�����ϸ��������δ�����Բ��죬��ȱѪ�ٹ�ע��Ͷ�������ȣ��������������ߣ���������ļ�ϸ��ȱѪ�ڣ�ϸ����������ϸ����������Ҫ��ʽ��������Ҫ�������ٹ�ע�����С�ʹ�ã𣳣��ͣ��У����Ƽ��ӣ£�������������ȱѪ�ٹ�ע���̵����������½���˵���𣳣��ͣ��У˵Ļ�ٽ���ϸ���ĵ��������ļ�ȱѪ�ٹ�ע����ϸ����������Ҫ�ź�;������ʹ�ã𣳣��ͣ��У˺����Ƽ����ϸ���������Ը���ȱѪ�飬�������ˣ𣳣��ͣ��У��ź�ͨ·����ϸ�����������⣬���������ź�ͨ·�����ļ�ϸ���ĵ������������Ƕ���ʵ��Ľ����һ�¡�
�����ļ�ȱѪ�ٹ�ע���˵Ļ��ƽϸ��ӣ��𣳣��ͣ��У˽�Ϊ�����ź�ת��;��֮һ��Ŀǰ�𣳣��ͣ��У˸�������Ӧ�Ĺ��ܼ�����ѧ�����в���ȷ��������Ӧ�������μ�ø�����õĵ����ʮ�������������ʵ��ƽ̨�Ĵ�����������룬���ţ𣳣��ͣ��У��ź�;�����ļ�ȱѪ�ٹ�ע�����еĻ��ƻ�Խ��Խ�����������źŴ���;��ˮƽ����ҩ���Ԥ��Ҳ��Ϊ�����ļ��ٹ�ע�����ṩ�����ֶΣ�ͬʱҲΪȱѪ�����༲���Ļ��������ṩ�µ�������˼·��
���������
�����ۣ��� ���棬����������С�����У����ͣ��У��źŴ���ͨ·�о���չ�ۣʣݣ���Ⱦ����֢������������������������������������������
�����ۣ��ݣǣȣ��ԣ��Ρ��ӣ��̣̣ԣ̣̣̣ţҡ��ӣ��ˣɣΣϣӣȣɣ͡��٣��������죮�𣳣� �ͣ��С�������塡������������������������������ɣɡ��������������壭��������䡡�����������ɣ졡���������ۣʣݣ��ʡ��ã��졡�£��죬����������������������������������
�����ۣ��ݣ̣ɡ��ǡ��ƣ��ɣͣԣɣ��ڡ��ӡ������ףɣ̣̣ɣ��͡��ã��ɣ��������������������������졡�����������������������䡡���������㡡��������������壭�������𣳣��ͣ��Уˡ��������������������桡�ȣ�𣲣��ۣʣݣ��������ʣУ������졡�ȣ�������ã��㡡�У������죬�������������������ȣ������ȣ�����
�����ۣ��ݣף��Σǡ��ͣ��ԣӣ��ɡ��¡��ͣ��ԣգңңţΣԣɣΣš��͡��ף��������죮�У��� ���������������������䡡��������������塡��������������������衡���������硡���䡡������������졡����������������塡�������ۣʣݣ������ԣ����㡡�ӣ���磬������������������������������������
�����ۣ��ݣӣԣţţҡ��͡��̣��ң�����������𡡣������������������������䡡��������������ۣʣݣ��ң����������У������죬������������������������������
�����ۣ��ݣӣȣɡ��ã����ΣģţңӣӣϣΡ��ң��ڣȣ��ϡ��أ��������죮�У�������������塡��桡����������塡������������������������������������������䡡�����������塡��������������������ۣʣݣ��У���������������������������������������������
�����ۣ��ݣˣ��ӣɣţҡ��ҡ������£գţΣϡ��ϡ��ƣ��̣ɣУӡ��ġ��ʣ��������죮�ԣ���壭����䡡������飭�������桡�𣳣����������������������䡡���������������������������������㡡�������������䡡����졡������衡����������硡��������ᣭ���������������������ۣʣݣ��ʡ��£��졡�ã�����������������������������������������������
�����ۣ��� ���죬������������ȣ��𣳣�˿��ԭ�����ø�鵼�����ļ�ȱѪ�ٹ�ע�����źŴ������о��ۣʣݣ��й�ѭ����־����������������������������������������