
缺血后处理(ischemic postconditioning,IPO)即通过在心肌的再灌注早期经过反复短暂的缺血与再灌注,能减少心律失常的发生,改善心功能,缩小梗死面积,减少心肌细胞凋亡[1]。
Murry等[2]提出的预处理不同,IPO是在缺血后、再灌注之前进行反复短暂的缺血与再灌注。IPO可对已发生的心肌缺血事件起到挽救的作用,弥补了不可预知缺血事件造成的慌乱,尽量减少心肌的损害,有其更大的应用前景。但对其机制的研究尚未有公认的结论,有待进一步研究。本研究通过建立兔在体心肌IPO模型[3],观察JAK-STAT通路在心肌IPO中的作用,进一步探讨IPO的机制问题。
1 材料与方法
1.1实验动物
新西兰大白兔,雌雄兼有,体质量2.5~3.0kg。将实验用兔(雌雄兼有)40只随机分为3组。组1(单纯缺血再灌注组,I/R组,n =10)进行简单的缺血再灌注,暴露左心 室前降支(LAD),以1号丝线于中上1/3处旁开1mm进针缝线,横穿LAD,另一端旁开1mm出线,剪针,套管,阻断LAD远端血流(以心电图ST段抬高为标志)30分钟后,开放120分钟。组2(单纯缺血后处理组,IPO组,n =10)于LAD的中上1/3阻断30分钟,开放后30秒再予阻断30秒,再开放,如此反复3次。
即进行IPO,随后再灌注120分钟。组3(AG490+IPO组,n =10)于阻断后10分钟给予酪氨酸激酶抑制剂AG490(1mg/kg),其他操作同组2。

1.2材料与试剂
AG490(美国SIGMA公司);Tunel试剂盒(德国宝灵曼公司);TKR-200c小动物呼吸机(江西特力麻醉呼吸设备公司);RM6240C生理信号采集系统(成都仪器厂);荧光显微镜 (日本Olympus公司);1.3数据采集以阻断前10分钟为起点,期间每10分钟记录1次左心室压力情况,以LSD(是一种文件格 式,由RM6240C系 统 自 动 生 成)文 件 保 存,RM6240C多道生理信号采集系统进行分析,所得数据保存于Excel表格中。每组分别于阻断即刻、阻断后20分钟、再灌注后60分钟、再灌注后120分钟抽取2ml血液作为标本,进行心肌磷酸激酶(CPK)的检测。最后处死动物,取缺血中心区心肌,裁减为黄豆大小置入4%多聚甲醛固定液和10%中性缓冲福尔马林固定溶液中保存,做好标记。固定48~72小时后进行常规石蜡包埋,进行Tunel检测观察细胞凋亡情况。
1.4统计学方法采用SPSS 17.0统计软件进行数据分析,实验数据均以均数±标准差(x-±s)表示,组间比较采用方差分析,不同时点间的比较采用重复测量的方差分析。
P <0.05表示差异有统计学意义。
2 结果
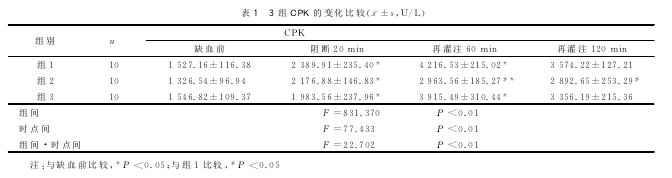
2.1 CPK的变化
不同组间差异有统计学意义(P<0.01),时点间差异有统计学意义(P <0.01),组别与时点间存在交互作用(P <0.01),进一步分析组间和时间的单独效应,各组的CPK于阻断后较缺血前明显增加(P <0.05),组1和组3再灌注120分钟 较60分钟下降,差异有统计学意义(P<0.05);组2CPK于再灌注60分钟和120分钟后较组1显著降低(P <0.05),而组3与组1再灌注后60分钟两者之间比较差异无统计学意义,结果见表1。
2.2心功能指标的变化
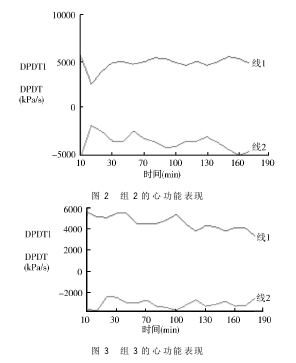
本实验以RM6240C多道生理信号采集系统分析了所记录的压力波形,通过该系统给出的参数,我们对左心室内压上升及下降最大速率(±dp/dt max,即在收缩期单位时间内左心室压力上升的最大速度,以“+”号表示,反映了心室的收缩功能;舒张期单位时间内心室压力下降的速度,以“-”号表示,反映左心室的舒张功能),采用SAS软件进行了LINEPLOT分析,以时间作为X轴,±dp/dt max作为Y轴(图1~3)。
±dp/dt max是反映左心室收缩功能及舒张功能的重要指标,越靠近0点表明心功能越差,对比组1与组2,可看出组1心功能呈下降趋势;而组2不明显,说明IPO对心功能起到了保护作用。组3波形也向0点靠近,说明AG490阻断了后处理的保护作用。
2.4心肌细胞凋亡变化
光镜下随机选取10个视野(×400)计数阳性细胞占视野中总细胞的千分率。
每张切片随机选取视野,计数100个细胞,并计数细胞核呈现棕黄色颗粒的阳性表达细胞,其总和即为这张切片心肌凋亡细胞的千分率。在镜下可以看到组1与组2的阳性率较高,并可见凋亡细胞经常簇集在一起;组3的心肌凋亡细胞相对较少。组2的细胞凋亡千分率均小于组1(P <0.01),组3与组1差异无统计学意义,见表2。
3 讨论
在缺血再灌注时进行IPO,激发机体的内源性心肌保护机制系统,最终结果起到了心肌保护的作用。但对于该机制是存在于器官、组织、细胞哪一级水平,作用于哪一条细胞通路,是一条或是多条通路相互起作用,人们先后提出了各种观点,比如抑制中性粒细胞活化[4-5],减少氧化剂介导的细胞损伤[2-4],抑制细胞内和线粒体内钙超载[5-6],激活再灌注损伤补救激酶途径(RISK)[6-9]等。本研究通过建立兔的心肌缺学后处理模型,研究JAK-STAT通路在兔心肌IPO中的作用,进一步探讨IPO的作用机制问题。
JAK-STAT通路是人们在研究干扰素(IFN-α、IFN-γ)对培养细胞基因转录的诱导作用时发现的,JAK和STAT都属于多成员家族。
JAK家族是一种非受体型酪氨酸蛋白激酶(PTK),其分子质量为120 000~130 000,有JAK1、JAK2、JAK3和TYK2等4个成员。该家族中的成员由7个功能域构成[10],JH1(JAK homology region 1)是有PTK催化活性的激酶功能域;JH2为激酶样功能域,由于缺乏激酶活化所必需的氨基酸残基而没有激酶活性,同时是与STAT结合的部位[11]。STAT是一种DNA结合蛋白,结构中含有SH2、SH3功能域。
STAT家族共有7个成员,即STAT1、STAT2、STAT3、STAT4、STAT5a、STAT5b和STAT6。其结构域中C端的酪氨酸磷酸化(Tyr-P)有助于形成同源或异源二聚体。
研究证实,细胞因子与细胞因子受体结合后,其受体的胞内部分发生二聚体化,JAK与二聚体化受体的box功能区结合并发生磷酸化而激活。活化的JAK进一步诱发二聚体受体复合物周围的PTK底物活化,包括细胞因子受体型PTK、JAK家族成员和STAT等。
STAT是JAK激酶底物,可通过SH2功能域与二聚体受体复合物的酪氨酸位点以及JAK上的KLD功能区域结合。
STAT的y功能域在JAK的作用下发生Tyr-P,STAT被激活。胞浆内活化的STAT通过SH2功能域形成同源或异源二聚体,如SIF-A(STAT3和P48等构成)、SIF-B(STAT3-STA T1)、SIF-C(STAT1-STAT1)等。这些二聚体通过特定的机制移位到细胞核内并进一步结合到相应靶基因的启动子上,启动基因表达[12-13]。
我们假设JAK-STAT通路在心肌的IPO中也发挥了一定的作用。本实验结果中组2较组1在心肌酶、心功能的变化、细胞凋亡等方面均有明显的改善,IPO确实起到了心肌保护作用,证明本实验成功复制了兔在体心肌缺血后处理模型。而组3与组2相比,在心肌酶、心功能的变化、细胞凋亡等方面均无明显的改善,说明AG490可以消除后处理的保护作用,而作为JAK-STAT通路的特异性抑制剂,AG490只能通过作用于JAK-STAT通路,由此可证明JAK-STAT通路在心肌的缺血后处理中也发挥了不可替代的作用。
2001年,Omura等[14]发现,在体心肌缺血时,血管紧张素(AngⅡ)信号是心肌JAK-STAT通路激活的主要原因。随后,Mascareno等[15]发现,缺血再灌注选择性激活STAT5a和STAT6,激活的STATs与血管紧张素原(angiotensinogen,Ao)基因启动子St结构域结合,上调Ao-mRNA的表达。
2000年,Kodama等[16]研究发现JAK2抑制剂AG490能够强烈抑制培养心肌细胞的ANP的 表达,表 明JAK-STAT通路参与了血管舒-缩活性肽的表达。这与本实验的结果一致,应用AG490后,IPO+AG490组的后处理的保护作用也被消除。
己有的证据表明,STAT 1和STAT3激活对心肌具有相反的作用,STAT 1的激活诱发凋亡,而STAT3激活却抑制凋亡,发挥心肌保护作用[17]。
Yamaura等[18]通过基因敲除小鼠研究发现,STAT5a敲除的小鼠其缺血预处理的保护作用消失,而STAT6敲除的小鼠其缺血预处理的保护作用仍然存在,说明STAT5a在缺血预处理中发挥了积极作用,而且证明STAT5a可以同时被JAK-STAT、Src Kinase两条途径激活,Src Kinase激活的STAT5a通过PI3K磷酸化Akt而达到心肌保护作用。结果表明JAK-STAT信号通路可以通过和其他通路的交谈(cross-talking)而发挥作用,这就增加了JAK-STAT通路的复杂性。
新近的研究表明,机体内存在多种下调JAK-STAT信号通路的调节途径,除受体入胞这种常见的信号下调途径外,至少有3个蛋白质家族抑制JAK-STAT信号通路:细胞因子信号抑制物(supressors of cytokine sibnalling,SOCS)、活 化STATs抑制蛋白 (PIAS protein inhibitors ofactivated STATs)和含有SH2结构域的磷酸酶(SHP SH2-containing phosphatase)[11,19]。SOCS蛋白家族共有7个成员,即SOCS1-SOCS7。SOCS蛋白家族是STAT激活的靶基因产物。
STAT激活诱导SOCS表达,表达的SOCS又以负反馈的形式抑制JAK-STAT信号通路的活化[19]。目前,SOCS蛋白家族对JAK-STAT信号通路的调节作用己被充分证实,但其发挥负反馈调节作用的确切机制尚未明了。
PIAS家族是一组能与STATs结合的蛋白质。日前己发现5个 成 员,PTAS1、PTAS3、PIASy、PIASxa、PIASxb。PIAS可与激活的STATs二聚体结合,阻断该二聚体与DNA结合。SHP是存在于细胞质中的磷酸酶。
SHP1,SHP2能使JAKS和STATs去磷酸化,从而发挥抑制JAK-STAT信号通路的作用。另一方面,机体内尚存在JAK-STAT信号通路的正调节机制,包括丝氨酸激酶和一些相互作用的蛋白质。
STATs羧基末端转录激活结构域含有一个丝氨酸残基,2001Kovarik等[20]研究发现,该丝氨酸残基磷酸化可增强STAT1、STAT3、STAT4的转录活性,提高部分靶基因的表达。此外,STATs还可以和其他的转录调节物相互作用,如:STAT1与NF-B、SP1、糖皮质激素受体等,从而构成了一个十分复杂的调节体系。
最后,我们可以认为:
①心肌缺血后处理可以减少心肌酶的释放,心肌细胞凋亡,改善心功能。
②JAK-STAT通路参与了缺血后处理的保护机制。但是JAK-STAT通路与其他通路的交汇作用,以及JAK-STAT家族中是否全部参与了IPO的保护机制还不清楚,有待于进一步的研究。





